LES CLES DU DIMENSIONNEMENT
Ouvrages en commandePhotovoltaïque autonome
Photovoltaïque raccordé au réseau

Formations Professionnelles Photovoltaïques
Influence du cuivre sur différentes espèces bactériennes connues pour coloniser les réseaux d’eaux > Autres bactéries
Escherichia coli
Escherichia coli (E. coli) est une bactérie fréquente du tube digestif de l’homme et des animaux à sang chaud. La plupart des souches d’E. coli sont sans danger. Certaines souches, cependant, comme les souches entérohémorragiques (ECEH), peuvent être à l’origine de toxiinfections alimentaires (TIA) graves. Le groupe ECEH comprend notamment le sérotype O157:H7 qui est le plus important en santé publique.
L’infection, qui se caractérise notamment par une diarrhée sanguinolente, peut entraîner le syndrome hémolytique et urémique (SHU ; défaillance rénale aiguë qui se développe chez environ 5% des patients infectés), principale cause d’insuffisance rénale chez l’enfant et responsable d’un taux de mortalité variant de 0,6 à 5% chez les personnes atteintes de ce syndrome. Bien que la majorité des contaminations soient dues aux infections alimentaires, il existe une part de contamination sous estimée par les eaux de distribution non chlorées, les eaux de piscine et des eaux de puits.
Des infections d’origine hydrique attribuables à des souches pathogènes d’E. coli ont été signalées épisodiquement. En 1975, plus de 2 000 personnes fréquentant un parc national des USA ont été infectées par une souche de groupe ETEC (entérotoxinogénique) suite à la consommation d’une eau dont la concentration en chlore résiduel était insuffisante en extrémité de réseau. Au début des années 90, une épidémie d’origine hydrique (243 personnes affectées, dont 32 hospitalisations et 4 décès) mettant en cause la souche O157 :H7, s’est produite dans une petite municipalité du Missouri (3 000 habitants) ; l’origine a été attribué à l’infiltration d’eau contaminée dans le réseau de distribution. En mai 2000, l’épidémie de Walkerton (Ontario) a mis en cause la souche O157 :H7 et Campylobacter jejuni. A la suite de la contamination de l’un des puits municipaux par des déjections de bovins, plus de 2 300 personnes auraient été affectées, dont 1 346 ont manifesté des signes cliniques et six sont décédées. E. coli est un indicateur certain de contamination fécale récente dans les réseaux de distribution de l'eau potable. Il est donc un bon indicateur de la présence possible de pathogènes entériques constituant un risque pour la santé humaine. Par conséquent, la présence d'E. coli dans un réseau d'eau potable doit être nulle dans 100mL, selon les recommandations de l'OMS et les normes de la plupart des pays.
L'équipe de Maule, Keevil et Rogers a déterminé les effets du cuivre et d’autres matériaux de canalisation sur la survie et la croissance d’E. coli O157.
Les coupons en polybutylène, cuivre et acier inoxydable sont incubés dans l’eau pendant 7 jours puis retirés pour l’évaluation des biofilms bactériens sur les surfaces.
Dans l’eau de faible dureté, les résultats indiquent qu’E. coli O157 ne faisait partie de la microflore à 40°C sur aucun des matériaux suggérant son incapacité à former des biofilm dans cette eau à cette température. Le recouvrement d’E. coli O157 était le plus important à 20°C. A 10°C, la concentration d’E. coli était réduite de 100 fois sur le cuivre comparé aux autres matériaux.
Dans l’eau de dureté moyenne, le plus grand nombre d’E. coli O157 a été retrouvé à 10°C. Comme avec les biomasses totales du biofilm dans l’eau douce, il n’y avait pas d’E. coli dans les biofilms établis dans l’eau modérément dure à 40°C suggérant que malgré sa survie dans la phase aqueuse à cette température, la souche utilisée est incapable de former un biofilm à cette température élevée.
E. coli O157 est retrouvé à 40°C indiquant que cette bactérie pathogène peut mieux survivre au sein des biofilms dans les eaux de plus forte dureté. Bien que le nombre d’E. coli O157 détecté soit très faible sur le cuivre et l’acier inoxydable à 40°C les auteurs en isolent 100 fois plus sur le polybutylène.
En eau de faible dureté, le cuivre est contaminé 10 à 100 fois moins par E. coli O157 que l’acier inoxydable. La plus grande contamination s’est produite sur le polybutylène.
E. coli O157:H7 colonise plus facilement le polybutylène que l’acier inoxydable et encore moins le cuivre. Malgré quelques exceptions, la tendance se répète pour tous types d’eau et à différentes températures.
Cependant cette étude est basée sur des observations de 7 jours d'incubation ce qui est trop faible pour garantir un état au moins métastable et il est difficile d’extrapoler cette période pour mesurer le temps de survie sur de longues périodes.
Domek et al. ont étudié l’impact des métaux sur Escherichia coli dans des conditions représentatives des systèmes de distribution d’eau. Des analyses ont été réalisées sur 44 échantillons d'eau potable recueillis dans deux réseaux d'eau potable à faible niveau de chlore résiduel. Des corrélations significatives au risque 5% ont été trouvées entre les altérations sur les bactéries (bactéries stressées ou "injured") dans l’eau potable et la température, le pH, le cuivre, et le carbone organique total.
Les auteurs indiquent que, par rapport aux paramètres température, pH, et carbone organique total, le cuivre peut contribuer au processus d’altération cellulaire et réduit significativement les dénombrements de coliformes. De plus, le potentiel de trois métaux (plomb, cadmium et cuivre) à endommager les cellules a été testé individuellement et les résultats montrent que le cuivre seul induit autant de dommages qu’un mélange de tous les autres métaux étudiés. Les lésions progressives des cellules d’E. coli causées par l’exposition au cuivre (0,05 et 0,025 mg/L) dans une solution tampon sont illustrés Figure 37. Plus de 90% des lésions se produisent après deux jours à 4°C avec 0,05 mg/ L de cuivre. Avec des temps de contact plus longs à cette concentration de cuivre, les cellules altérées commencent à mourir, suite à la faible diminution des lésions observée au 7ème jour. A des concentrations de cuivre plus faibles (0,025 mg/L), les lésions progressent plus lentement, prenant 6 jours à atteindre le niveau de 90%. Les températures plus élevées accélèrent le niveau d’endommagement causé par le cuivre. Bien qu’un nombre limité d’expérimentations ait été réalisé, le temps nécessaire pour induire 90% des stress à 0,05 mg/L de cuivre était seulement d’1 jour à 22°C. De plus, des concentrations plus élevées (0,25 mg/L) provoquent des dégâts plus rapidement (< 1 jours à 4°C), mais de grandes diminutions dans la viabilité de cellule ont été aussi observées.
Assanta et al. (57) observent au microscope électronique à balayage, l’adhésion d’Escherichia coli O157:H7 sur des surfaces de canalisations de distribution d’eau en cuivre et polyéthylène à différents temps de contact et températures. Des coupons stériles des deux matériaux ont été plongées dans un récipient contenant 5 mL d’une suspension bactérienne de 2 x 108 UFC/mL avec des temps de contact de 1, 4, 24, 48 et 72 heures à des températures de 4°C et 20°C.
A l'oeil, les deux matériaux apparaissent très lisses. Pourtant, d’après l'observation au microscope électronique à balayage (Figure 38), la surface en cuivre est souvent marquée par les éléments rugueux comme des grains et des crevasses dans lesquelles des bactéries pourraient être capables de se loger, alors que le polyéthylène présente une surface irrégulière.
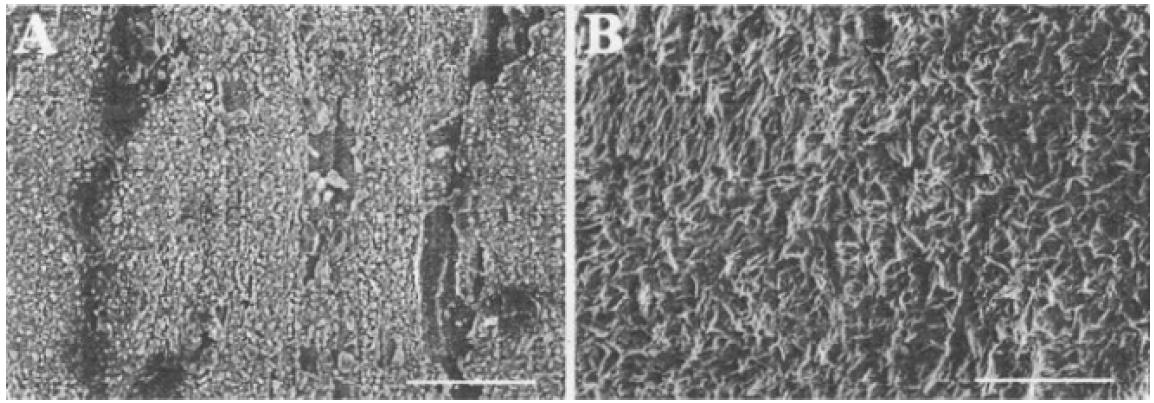
Aperçu de la structure de surfaces non contaminées (A) cuivre et (B) polyéthylène
Les figures suivantes montrent que la surface en cuivre après incubation est couverte par un nombre élevé de cellules Escherichia coli en comparaison à celle en polyéthylène. Cependant, le nombre croissant de cellules, sur chacune des surfaces montre l’influence du temps et de la température sur l’exposition d’attachement de cet organisme entéropathogénique.
Finalement, les observations au microscope électronique à balayage révèlent qu’E. coli peut se fixer aux deux surfaces après 1 h d’exposition, que la colonisation par ce microorganisme est plus importante à 20°C (images C et D) qu’à 4°C (images A et B), et que les cellules sur le matériau cuivre apparaissent lésées après 72 h d’attachement (images A et C).
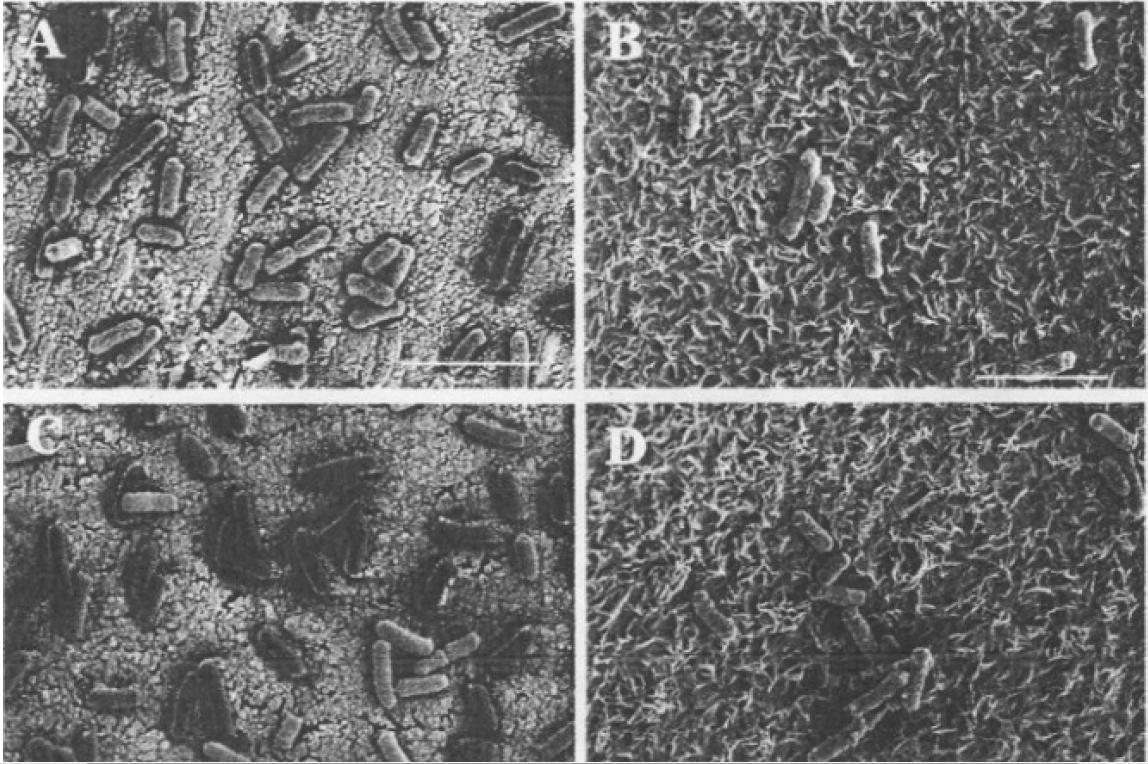
Observation au microscope électronique à balayage des cellules d’Escherichia coli fixées sur le cuivre (A, C) et le plastique (B et D) après 24 h de temps de contact à 4°C (A et B) et 20°C (C et D)
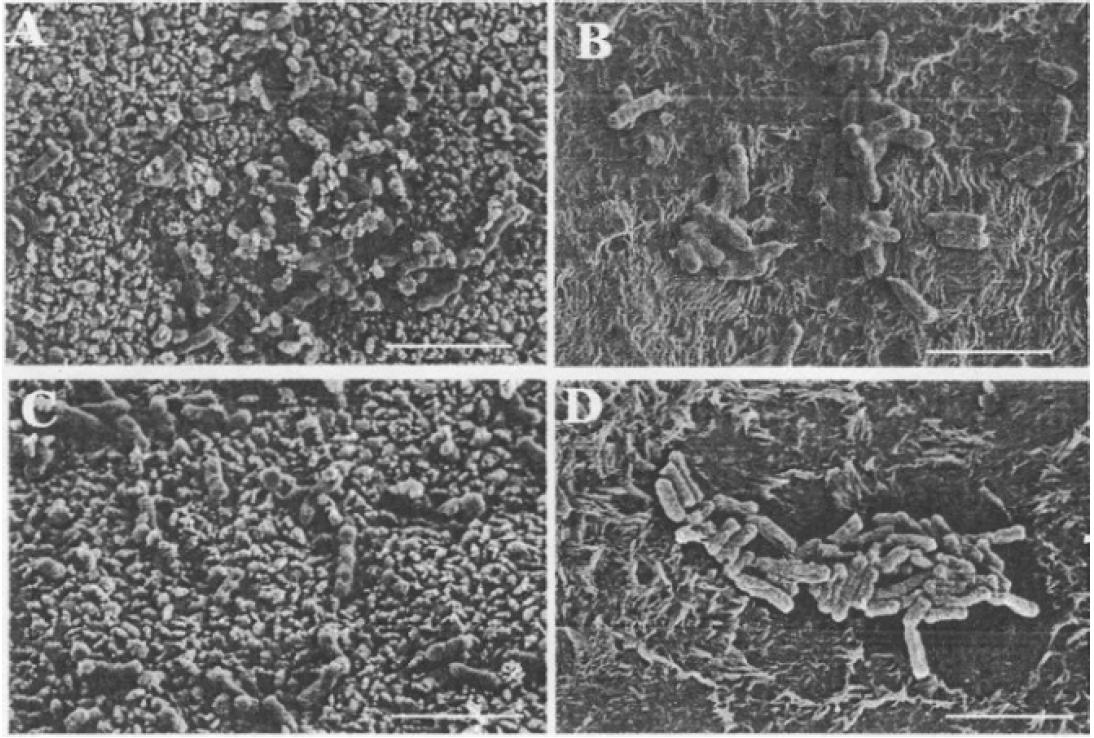
Observation au microscope électronique à balayage des cellules d’Escherichia coli fixées sur le cuivre (A, C) et le plastique (B et D) après 72 h de temps de contact à 4°C (A et B) et 20°C (C et D)
Il existerait, selon les auteurs, une relation entre les irrégularités de surface des matériaux inertes et la capacité d’E. coli O157:H7 à se fixer à cette même surface particulière.
L’altération des cellules d’E. coli sur le cuivre après 72 h suggère que les ions cuivriques présentent un effet antimicrobien sur cette bactérie.
Silhan et al. ont étudié la survie d’E. coli dans les biofilms et dans l’eau dans des segments de canalisation d’eau potable en acier galvanisé, en polyéthylène réticulé, en cuivre et en polyéthylène de densité moyenne. Les tubes remplis ont été incubés à 15°C ou 35°C en statiques. A 15°C, E. coli survit plus de 4 jours dans l’acier galvanisé et le cuivre et 8 jours dans les canalisations en polyéthylène, mais n’est pas détectable après 48 h à 35°C.
Conclusion > Bactérie Escherichia coli
Bien que l'étude microscopique montre une colonisation plus élevée du cuivre par la souche d'Escherichia coli utilisée, la tendance globale des résultats publiés montre que le cuivre est le matériau comportant globalement une plus faible biomasse par rapport aux autres testés dans les mêmes conditions. De plus, le cuivre semble avoir un effet antimicrobien direct sur les cellules d’E. coli et inhibe ainsi leur développement.
Helicobacter pylori
Helicobacter pylori (H. pylori) est une bactérie flagellée Gram négatif qui est l’agent étiologique de l’ulcère gastrique et duodénal. Ce germe, d'habitat digestif (muqueuse digestive), est un germe spiralé et mobile, micro-aérophile et de croissance lente se retrouvant aussi sous forme bacillaire ou coccoïde.
Sa transformation vers la forme coccoïde peut être induite par une exposition du microorganisme à des conditions sous optimales, telle que la privation de nutriments ou une incubation prolongée, suggérant que ces formes sont un stade dormant d’H. pylori et peuvent constituer une stratégie de survie dans des conditions hostiles de l'environnement. La forme spiralée est habituellement associée aux formes infectieuses de la bactérie.
Pour l'instant, l’origine environnementale et le mécanisme de transmission à l’humain hôte ne sont pas clairement établis. Cependant, il a été mis en évidence que l'eau est un des véhicules de l'infection.
Ce micro-organisme a la capacité à s’incorporer dans les biofilms en laboratoire et a également été détecté dans des biofilms de réseaux en utilisant des techniques moléculaires.
Azevedo et al. (73) ont essayé d'établir dans quelle mesure Helicobacter pylori est capable de se fixer à différents matériaux communément utilisés dans les systèmes d'eau potable et si des différences dans la morphologie cellulaire et la capacité à former des agrégats pourraient être trouvées pour les différents matériaux.
Des coupons de 2 x 2 cm de cuivre, PVC, polypropylène et de verre ont été désinfectés puis contaminés par une suspension de H. pylori. A différents temps d’exposition, un coupon de chaque matériau est retiré. Les cellules, marquées au Syto9 et à l’iodure de propidium, sont dénombrées au microscope à épifluorescence.
Les résultats montrent que toutes les surfaces ont été colonisées par H. pylori, avec approximativement 75% du nombre total de la situation d'équilibre obtenues à la fin des 48 premières heures d’exposition. Entre 96 et 192 heures, le nombre total de cellules reste à peu près constant pour tous les matériaux excepté le polypropylène.
A l'état d'équilibre, il n'existe pas de différence significative entre les matériaux.
La proportion de bactéries coccoïdes varie clairement selon le matériau. Alors que pour les matériaux polymériques, tels que le polypropylène et le polychlorure de vinyle, la morphologie coccoïde ou en forme de U représente 80-90% du nombre total de cellules après 48 heures d’exposition, et approximativement 95% après 192 heures, pour le cuivre ces chiffres n’excèdent jamais 50% même après 192 heures (Figure ci-dessous). Pour le reste des matériaux, le verre, SS316 et SS304 la proportion de cellules coccoïdes après 192 heures atteint entre 70 et 85%.
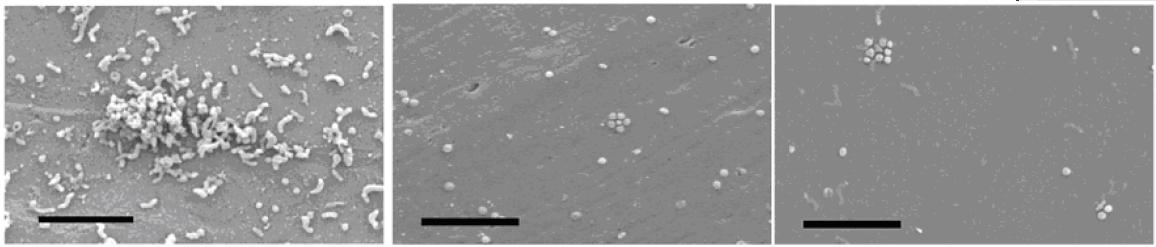
Observation au microscope électronique à balayage des cellules d’Helicobacter pylori fixées après 192 heures au cuivre (image du haut), au PVC (image du milieu) et au verre (image du bas)
Différents matériaux induisent différentes réponses sur Helicobacter pylori en termes de morphologie cellulaire. Comme la forme spiralée est usuellement associée avec une forme plus active de la cellule, la maintenance plus longue de la morphologie spiralée d’H. pylori lorsqu’il adhère aux surfaces de cuivre peut signifier que le cuivre procure une sorte de microenvironnement protecteur ou des nutriments essentiels au pathogène. En effet, H. pylori fait partie des quelques bactéries à posséder un système transporteur de cuivre, qui peut suggérer une plus grande tolérance des bactéries pour ce métal.
Le maintien de la forme spiralée sur le cuivre peut aussi être interprétée comme un effet rapide biocide du métal sur le pathogène, tuant la cellule avant qu’elle n’ait le temps de changer de forme.
Durant cette expérience, de larges agrégats sont retrouvés adhérents aux matériaux, spécialement sur le cuivre.
Le fait que le pathogène soit capable d’adhérer, de conserver la forme spiralée et de former de larges agrégats quand il adhère aux différents matériaux de plomberie, montre que les canalisations en général et en particulier celles en cuivre sont un réservoir possible de virulents Helicobacter pylori dans les systèmes de distribution d’eau.
Mycobacterium avium
Norton et al. ont conçu un réseau pilote pour examiner l’impact des niveaux de nutriments, des matériaux de canalisation, et de la désinfection sur la survie de Mycobacterium avium dans les biofilms. Le système se compose de canalisations en cuivre, cPVC, acier galvanisé, ou fer.
Après 11 semaines de croissance, le nombre de M. avium était significativement plus élevé sur le fer et les surfaces galvanisées que sur les surfaces en cuivre ou en cPVC.
Après 12 semaines de test, du chlore libre est additionné au système diminuant la teneur en bactéries hétérotrophes sur toutes les surfaces des canalisations excepté celles en fer, alors qu’une diminution du recouvrement de M. avium est notée pour toutes les surfaces. Après la décontamination, un pourcentage élevé de bactéries isolées sont des M. avium (95% sur le fer, 100% sur le cuivre).
Un autre système pilote a été conçu pour étudier les effets combinés des niveaux de nutriments, des matériaux de canalisation, et de la désinfection sur la survie de Mycobacterium avium dans les biofilms dans un système de distribution. Les résultats montrent que les niveaux de bactéries hétérotrophes des biofilms sur les surfaces en cuivre sont 3-4 log/cm² plus faibles que ceux des biofilms sur les surfaces en fer.
Les quantités de Mycobacterium avium dans les biofilms sont plus élevées sur le fer et l'acier galvanisé que sur le cuivre ou le cPVC. Significativement, quand les surfaces en cuivre sont exposées aux désinfectants, le pourcentage d’organismes identifiés comme M. avium augmente de quasiment 100%. Ces données indiquent que la désinfection de l’eau potable seule ne peut être efficace pour contrôler les biofilms de M. avium.
Conclusion > Bactérie Mycobacterium avium
Selon cette unique publication et, selon le protocole suivi, le cuivre et le cPVC sont moins colonisés par Mycobacterium avium que le fer ou l'acier galvanisé.
Aeromonas hydrophila
Ces dernières années, Aeromonas hydrophila a été reconnu comme un pathogène préoccupant identifié à l'origine de plusieurs infections humaines, incluant des gastroentérites, des péritonites, des endocardites, des méningites, des septicémies et des infections urinaires.
Cet organisme est communément distribué dans l’environnement, particulièrement dans les systèmes aquatiques aussi bien dans les lacs, rivières, que dans l’eau potable.
Assanta et al. ont étudié au microscope électronique à balayage la fixation d’Aeromonas hydrophila aux surfaces en fer, en cuivre et en polybutylène à des températures et des temps de contact différents. Des échantillons stériles d’acier inoxydable et de cuivre ont été totalement immergés, alors que les surfaces en polybutylène ont été trempées verticalement, dans une fiole de 5 mL contenant de la suspension bactérienne, avec des temps de contact de 1, 4, 24, 48 et 72 heures à température ambiante (20°C) et réfrigérée (4°C).
Les résultats montrent que l’acier inoxydable est recouvert par un nombre modéré de cellules, en comparaison au cuivre qui est colonisé par peu de cellules, malgré la durée d’exposition (après 1 heure). Dans tous les cas, la prolifération des cellules d’A. hydrophila sur la surface en cuivre est difficile à évaluer avec précision car les cellules apparaissent mortes. L’altération de la fixation des cellules est également observée. Quant au polybutylène, beaucoup plus de cellules d’Aeromonas sont observées fixées à cette surface, particulièrement si le temps de contact est prolongé.
Le plus grand nombre de cellules fixées est retrouvé sur le polybutylène, suivi par l’acier inoxydable, alors que peu de cellules sont observées sur le cuivre. L’altération des cellules fixées aux surfaces en cuivre indique les différences dans le comportement électrochimique de ce matériau.