LES CLES DU DIMENSIONNEMENT
Ouvrages en commandePhotovoltaïque autonome
Photovoltaïque raccordé au réseau

Formations Professionnelles Photovoltaïques
Sélection des fluides frigorigènes à faible impact environnemental > Les approches utilisées pour la classification par le niveau d’inflammabilité
Les mélanges des fluides frigorigènes modérément inflammables présentent un intérêt substantiel dû aux faibles valeurs de GWP des molécules ayant un faible nombre d’atomes de fluor et/ou un grand nombre d’atomes d’hydrogène.
Les fluides frigorigènes sont actuellement classés selon la norme américaine ASHRAE Standard 34 [ASHRAE, 2001]. Cette classification consiste en 3 classes d’inflammabilité définies par deux critères : la limite inférieure d’inflammabilité (LII) et le pouvoir calorifique (PC). Les 3 classes sont définies comme suit :
- classe 1 pour les fluides frigorigènes où aucune propagation de flamme n’existe quand ils sont testés avec l’air à 101 kPa et 21 °C selon ASTM E681-01 ;
- classe 2 pour les fluides frigorigènes qui possèdent une LII > 0,10 kg/m3 à 21 °C et 101 kPa et un PC < 19 000 kJ/kg ;
- classe 3 pour les fluides frigorigènes qui possèdent une LII < 0,10 kg/m3 à 21 °C et 101 kPa ou un PC > 19 000 kJ/kg
Cependant, cette classification présente certains défauts et plusieurs frigorigènes sont mal classés en utilisant ces deux seuls critères. De nouvelles contributions pour une classification plus cohérente sont donc nécessaires. Ces contributions ont proposé de nouveaux indices introduisant l’intensité de la réaction : R-index [Kataoka, 2001], la probabilité d’allumage : RF-number [Kondo, 2002] et la vitesse fondamentale maximale de flamme : RF2-number [Jabbour, 2004; Kondo, 2004].
Tous ces indices nécessitent au moins la détermination des limites d'inflammabilité et du pouvoir calorifique. Dans cette étude, le nombre RF-number combinant les deux facteurs de probabilité et d’intensité d’allumage est utilisé. Dans la limite des mélanges formés par les corps purs choisis, ce facteur formulé par l’équation (3.1) permet une classification assez pertinente [Kondo, 2002] :
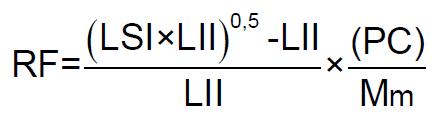
Avec :
- LII et LSI les limites inférieure et supérieure d’inflammabilité,
- PC le pouvoir calorifique (ou chaleur de combustion) en [J/mol],
- Mm la masse molaire en [g/mol].
Pour cette évaluation, les mélanges seront classés comme étant modérément inflammables pour un RF inférieur à 30 et hautement inflammables pour un RF supérieur à 30 [Kondo, 2002].
Calcul des limites inférieures et supérieures d’inflammabilité (LII et LSI)
Pour un mélange d’hydrocarbures ou de corps inflammables, les limites d'inflammabilité peuvent être directement estimées par la loi de Le Chatelier exprimée par l’équation ci-après. Ceci contrairement aux mélanges composés de corps inflammables et non inflammables où il est préférable d’utiliser des données expérimentales car la prédiction précise des limites d'inflammabilité est une tâche difficile.
La loi de Le Chatelier est exprimée par :
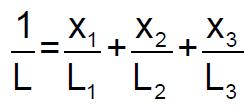
Avec :
- x1, x2 et x3 les fractions molaires des composants du mélange
- L1, L2 et L3 les limites d'inflammabilité respectives.
Un modèle de calcul [Zhao, 2004], basé sur les données expérimentales d’inflammabilité des différentes combinaisons binaires possibles des corps choisis, composés d’un corps inflammable et d’un autre non inflammable, est utilisé pour une classification rapide en deux groupes : inflammable et non inflammable. Cette méthode permet de calculer les limites inférieures et supérieures d’inflammabilité des mélanges formés de trois corps purs ou plus, inflammables ou non inflammables, à partir des données expérimentales des mélanges binaires. Les régressions polynomiales de ces données sont introduites dans le modèle de calcul (courbe de la figure ci-après).
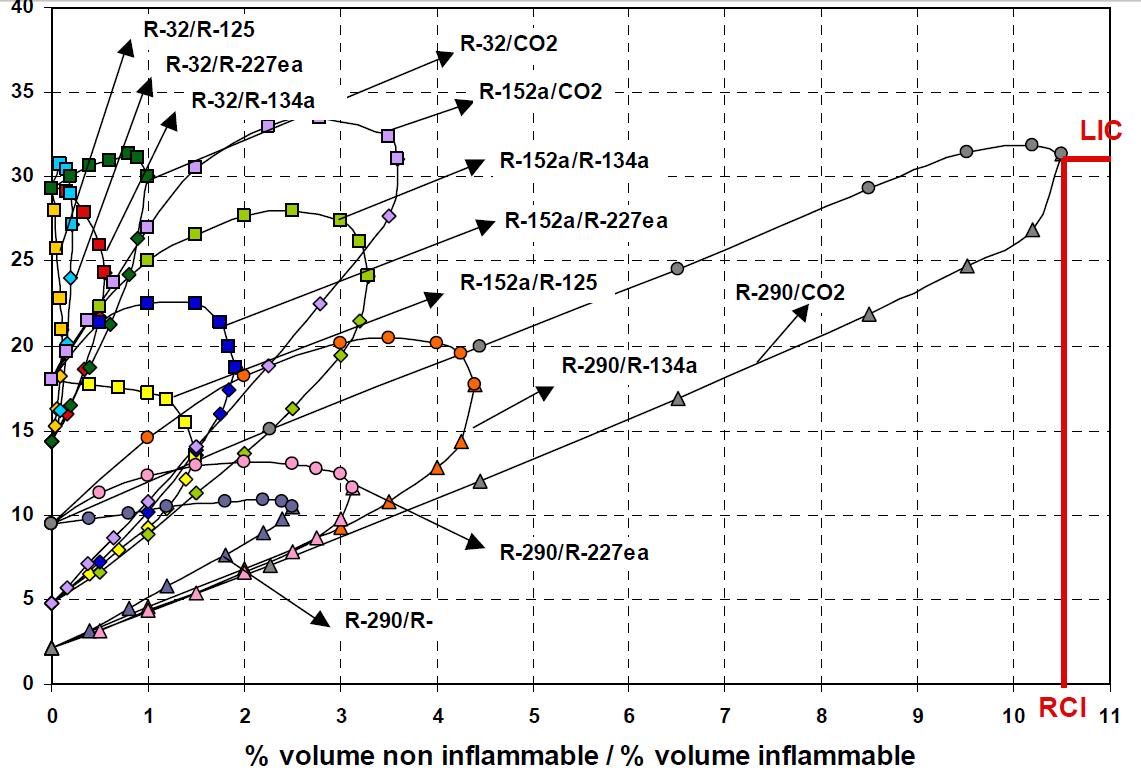
Régressions des données expérimentales des LII et des LSI
Le HC-290, le HFC-125 et le HFC-32 choisis pour cette évaluation sont listés dans le tableau 1. Les tableaux 2 et 3 donnent respectivement les valeurs de la limite d’inflammabilité critique et du rapport critique d’inflammabilité. Le rapport critique d’inflammabilité est égal au rapport entre le volume du corps non inflammable et le volume du corps inflammable correspondant à la limite d’inflammabilité critique. Les mélanges présentant des rapports supérieurs au rapport critique sont considérés non inflammables.
La limite d’inflammabilité critique est la valeur de la LII ou de la LSI pour un rapport non inflammable/inflammable égal au rapport critique.
| LII (% vol) | LSI (% vol) | PC (MJ/kg) | Cst (%vol) | |
|---|---|---|---|---|
| R-290 | 2,1 | 9,5 | 50,3 | 4,0 |
| R-152a | 4,8 | 18,0 | 17,4 | 7,7 |
| R-32 | 14,4 | 29,3 | 9,4 | 17,4 |
| Tableau 1 - Critères d’inflammabilité des corps inflammables LII : limite inférieure d’inflammabilité, LSI : limite supérieure d’inflammabilité PC : pouvoir calorifique inférieur, Cst : concentration stoechiométrique dans l’air |
||||
| LIC [%] | R-744 | R-134a | R-125 | R-227ea |
|---|---|---|---|---|
| R-290 | 31,3 | 17,7 | 10,5 | 11,6 |
| R-152a | 31,0 | 24,2 | 13,5 | 18,7 |
| R-32 | 30,0 | 24,3 | 21,0 | 27,1 |
| Tableau 2 - Limites d’inflammabilité critiques des binaires inflammable/non inflammable LIC : limite d'inflammabilité critique |
||||
| RCI | R-744 | R-134a | R-125 | R-227ea |
|---|---|---|---|---|
| R-290 | 10,50 | 4,40 | 2,50 | 3,12 |
| R-152a | 3,60 | 3,30 | 1,50 | 1,91 |
| R-32 | 1,00 | 0,55 | 0,11 | 0,22 |
| Tableau 3 - Rapports critiques d’inflammabilité des binaires inflammable/non inflammable RCI : rapport critique d’inflammabilité |
||||
Le HFC-32 et le HFC-152a sont classés modérément inflammables par l'ASHRAE 34, le CO2 avec un GWP de 1 a un effet de dilution et le R-125 et le R-227ea à GWP relativement élevé sont de bons extincteurs. Le R-290 très inflammable présente des performances élevées et le R-134a moins extincteur que le R-125, possède un GWP acceptable pour cette application en 2006.
Mélanges de deux composants inflammables et d’un composant non inflammable
Supposons que A, B et C soient les trois composants d'un mélange, A et B sont inflammables et C est non inflammable. La méthode de calcul des limites inférieures et supérieures d’inflammabilité L dépend des concentrations des corps non inflammables dans le mélange. Trois cas sont identifiés.
Cas 1
Si les rapports molaires de C sur A et de C sur B sont inférieurs aux rapports d’inflammabilité critiques des binaires (C,A) et (C,B) respectivement, C avec A ou B peut former un nouveau mélange. Les limites d'inflammabilité de ce mélange peuvent donc être trouvées en se référant aux courbes expérimentales des limites d'inflammabilité (cf. figure précédente). La limite d'inflammabilité L du mélange est ensuite calculée par l’équation suivante :
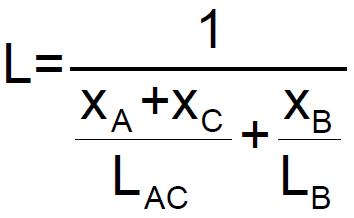
Avec :
- xA, xB et xC lsont les fractions molaires de A, B et C respectivement,
- LAC la limite d'inflammabilité du binaire (A,C),
- LB la limite d'inflammabilité de B.
Cas 2
Si le rapport molaire de C sur A est supérieur au rapport d’inflammabilité critique du binaire correspondant et le rapport de C sur B est inférieur au rapport d’inflammabilité critique du binaire (C,B), un nouveau mélange peut se former par le composant non inflammable C et le composant inflammable B. Les limites d'inflammabilité de ce mélange peuvent donc être trouvées par la même équation que le cas 1.
Cas 3
Si les rapports molaires de C sur A et de C sur B sont supérieurs aux rapports d’inflammabilité critiques des binaires (C,A) et (C,B) respectivement, C est divisé en deux parties de façon à ce que le rapport d’une partie de C sur A ou B soit égal au rapport critique correspondant. La fraction molaire du corps non inflammable C peut être définie par :
xC = xCAR + xΔC
Avec :
Avec :
- xCAR est la fraction molaire de C lorsque le mélange (A,C) atteint le rapport critique
- xΔC est la fraction molaire restante de C.
Si xΔC / xB > RBC, alors le mélange est non inflammable
Si xΔC / xB ≤ RBC, alors les limites d'inflammabilité de ce nouveau mélange peuvent être trouvées en se référant aux courbes expérimentales des limites d'inflammabilité (cf courbes précédentes "Régressions des données expérimentales des LII et des LSI"). L sera ensuite calculé par l’équation :
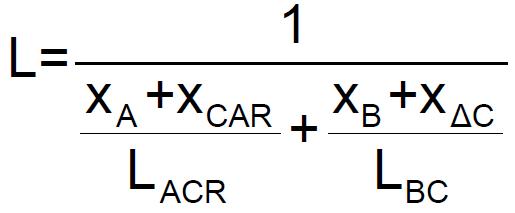
Avec :
- LACR est la limite d'inflammabilité critique du binaire (A,C),
- LBC la limite d'inflammabilité du binaire (B,C),
- RBC = xCBR / xB.
Mélanges de deux composants non inflammables et d’un composant inflammable
Supposons que A, C et D soient les trois composants du mélange, C et D sont non inflammables et A est inflammable. Le composant A est divisé en deux parties de façon à ce que le rapport d’une partie de A sur C ou D soit égal au rapport critique correspondant.
La fraction molaire du corps inflammable A peut être définie par :
xA = xADR + xΔA
Avec :
Avec :
- xADR est la fraction molaire de A lorsque le mélange (A,D) atteint le rapport d’inflammabilité critique
- xΔA est la fraction molaire restante de A.
Si xC / xΔA > RAC, alors le mélange est non inflammable
Si xC / xΔA ≤ RAC, alors les limites d'inflammabilité de ce nouveau mélange peuvent être trouvées en se référant aux courbes expérimentales des limites d'inflammabilité (cf courbes précédentes "Régressions des données expérimentales des LII et des LSI"). L sera ensuite calculé par l’équation :
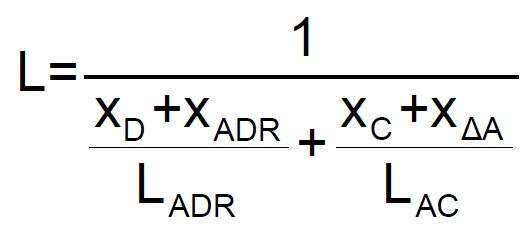
Avec :
- LADR est la limite d'inflammabilité critique du binaire (A,D),
- LAC la limite d'inflammabilité du binaire (A,C),
- RAC = xCAR / xA.
Calcul du pouvoir calorifique (PC)
Le calcul du Pouvoir Calorifique (PC) d’un mélange de fluides frigorigènes nécessite la détermination des équations stoechiométriques correspondantes. Les produits résultant de la combustion doivent être connus en fonction des réactifs et de leur concentration dans le mélange.
D’après Takizawa [Takizawa, 2005], les produits de la combustion doivent être HF, CO2 (N2, SO2 si l'azote et le soufre font partie de la structure moléculaire des frigorigènes) et HCl s’il y a suffisamment d’hydrogène dans la molécule. L’excès de H est considéré converti en H2O. La formation de HF devance la formation de HCl s’il y a insuffisamment d’H pour la formation de HF et HCl mais suffisamment pour la formation de HF. Dans le cas où le H est insuffisant pour la formation du HF, le F restant produit le COF2 puis le CF4 de préférence à la formation du CO2, le Cl restant produit de Cl2.
Le modèle utilisé pour le calcul du PC prend en considération ces différents éléments permettant ainsi de déterminer les produits de la réaction de combustion stoechiométrique d’un mélange d’un, de deux ou de trois corps purs inflammables ou non inflammables ainsi que le nombre de moles de chaque produit résultant par la résolution d’un système d’équations à l’aide du SOLVEUR du Logiciel EXCEL programmé en langage VISUAL BASIC.
Tous les fluides frigorigènes utilisés dans cette étude ont leur molécule de la forme CnHmFp.
Dans ce cas, le rapport H/F servira d'indice pour le choix des produits :
- si H/F est inférieur à 1, les produits de la réaction sont : CO2, HF, COF2, CF4 et N2
- si H/F est supérieur à 1, les produits de la réaction sont : CO2, HF, H2O et N2
x1. Cn1Hm1Fp1 + x2. Cn2Hm2Fp2 + x3 Cn3Hm3Fp3 + x4. CO2 + D. (O2 + 3,76 N2) → a. CO2 + b. HF + c. CF4 + d. COF2 + e. H2O + f. N2
Si x1.m1 + x2.m2 + x3.m3 > x1.p1 + x2.p2 + x3.p3 ⇒ H > F
Les équations à résoudre sont :
- Les produits sont CO2, HF, H2O et N2 : c = d = 0
- Equilibre des atomes C : x1.n1+x2.n2+x3.n3+x4 = a
- Equilibre des atomes H : x1.m1 + x2.m2 + x3.m3 = b + 2e
- Equilibre des atomes F : x1.p1 + x2.p2 + x3.p3 = b
- Equilibre des atomes O : 2x4 + 2D = 2a + e
- Equilibre des atomes N : 7,52 D = 2f
Si x1.m1 + x2.m2 + x3.m3 < x1.p1 + x2.p2 + x3.p3 ⇒ H < F
Les équations à résoudre sont :
- Les produits sont CO2, HF, COF2, CF4 et N2 : e = 0 et c < d
- Equilibre des atomes C : x1.n1+x2.n2+x3.n3+x4 = a + c + d
- Equilibre des atomes H : x1.m1 + x2.m2 + x3.m3 = b
- Equilibre des atomes F : x1.p1 + x2.p2 + x3.p3 = b + 4c +2d
- Equilibre des atomes O : 2x4 + 2D = 2a + d
- Equilibre des atomes N : 7,52 D = 2f
Le pouvoir calorifique (PC) est ensuite calculé en déduisant les enthalpies de formation des produits des enthalpies de formation des réactifs.
Le tableau suivant montre les résultats obtenus du pouvoir calorifique et du RF-number par le modèle et les valeurs publiées par Kondo [Kondo, 2002].
| PC (kJ/mole) | RF-number | |||
|---|---|---|---|---|
| Modèle | Kondo | Modèle | Kondo | |
| R-32 | 9400 | 9195 | 4,13 | 4,55 |
| R-152a | 16183 | 16500 | 15,15 | 14,9 |
| R-290 | 46300 | 46351 | 52,23 | 52,2 |
| Comparaison du PC et du RF-number | ||||