LES CLES DU DIMENSIONNEMENT
Ouvrages en commandePhotovoltaïque autonome
Photovoltaïque raccordé au réseau

Formations Professionnelles Photovoltaïques
Comportement de l'ozone dans les environnements intérieurs > Réactivité de l’ozone en phase homogène
Plus de 900 COV et aldéhydes ont été détectés dans les environnements intérieurs [Brown, 1999]. Pour la plupart de ces composés, leurs concentrations intérieures sont supérieures à celles de l’air extérieur. Lors de la campagne pilote de l’OQAI, les rapports de concentrations intérieures sur les concentrations extérieures de certains composés ont atteint des facteurs 14 et 17, réciproquement pour le d-limonène et l’hexaldéhyde [OQAI, 2002]. Des niveaux dix à vingt fois plus importants sont classiquement observés à l’intérieur. L’air intérieur constitue donc un microenvironnement où de nombreux composés sont rencontrés. Le Tableau suivant liste les principaux COV et aldéhydes retrouvés à l’intérieur ainsi que leurs sources identifiées [Brown, 1999 ; Maroni et al., 1995].
| Sources | Composés | |||
|---|---|---|---|---|
| Produits de consommation | hydrocarbures aliphatiques (n-décane, alcanes ramifiés), aromatiques (toluène, xylène), halogénés (chlorure de méthylène) ; alcools ; cétones (acétone, méthyléthylecétone) ; aldéhydes (formaldéhyde) ; esters (alkyl éthyoxylate) ; éthers (éther de glycol) ; terpènes (limonène, alpha-pinène) | |||
| Peintures et solvants | hydrocarbures aliphatiques (n-hexane, n-heptane), aromatiques (toluène), halogénés (chlorure de méthylène ; dichlorure de propylène) ; alcools ; cétones (méthyléthyl cétone) ; esters (éthylacétate) ; éthers (méthyl-, éthyl- et butyléther) | |||
| Adhésifs | hydrocarbures aliphatiques (hexane, heptane), aromatiques, halogénés ; alcools ; amines ; cétones (acétone, méthyléthyle cétone) ; esters (vinylacétate) ; éthers. | |||
| Fournitures et vêtements | hydrocarbures aromatiques (styrène, aromatiques bromés), halogénés (chlorure de vinyle) ; aldéhydes (formaldéhyde) ; esters ; éthers. | |||
| Matériaux | hydrocarbures aliphatiques (n-décane, n-dodécane), aromatiques (toluène, styrène, éthylbenzène), halogénés (chlorure de vinyle) ; aldéhydes (formaldéhyde) ; cétones (acétone, butanone) ; éthers ; esters (uréthane, éthylacétate). | |||
| Agents de combust | hydrocarbures aliphatiques (propane, butane, isobutane) ; aldéhydes (acétaldéhyde, acroléine) | |||
| Eau potable | hydrocarbures halogénés (1,1,1-trichloroéthane ; chloroforme, trichloroéthane) | |||
| Exemples de COV et leurs sources dans les environnements intérieurs | ||||
Conditions de réactivité
L’ozone peut réagir avec beaucoup de substances chimiques présentes dans l’air. Afin d’étudier la réactivité de l’ozone en phase gazeuse, il est nécessaire de prendre en compte les conditions thermodynamiques, cinétiques, les concentrations des espèces et le TRA [Weschler, 2000].
Malgré leurs caractéristiques thermodynamiques favorables, les réactions impliquant l’ozone sont cinétiquement limitées dans les environnements intérieurs. A température ambiante et aux niveaux de concentrations d’ozone rencontrés, elles sont trop lentes pour entraîner une diminution significative de la concentration d’ozone [Weschler, 2000]. En effet, des concentrations d’ozone comprises entre 100 et 200 µg·m-3 auront un impact négligeable sur la plupart des composés présents dans l’air intérieur. Par exemple, un temps supérieur à une année est nécessaire pour que 100 µg·m-3 d’ozone fasse diminuer de moitié la concentration des COV fréquemment observés dans les environnements intérieurs tels que l’hexane, le benzène, le xylène, l’acétone, la 2-butanone, le nonanal, le toluène et le 1,2-dichloroéthylène.
Il existe cependant des COV dont les temps de réaction sont suffisamment rapides pour contrebalancer l’effet du taux de renouvellement de l’air. Il s’agit en particulier des alcènes et notamment de l’isoprène, du styrène et des terpènes tels que l’alpha-pinène et le d-limonène dont les constantes de réaction sont égales à 7,3·10-4 et 1,7·10-3 µg-1·m3·min-1 réciproquement [Weschler, 2000]. Ces composés insaturés représentent 5 à 10% des composés organiques présents dans l’air intérieur [Brown et al., 1994]. Lors de la campagne pilote de l’OQAI, les COV majoritairement retrouvés dans les logements étaient l’alpha-pinène et le d-limonène [OQAI, 2002].
Ces composés susceptibles de réagir avec l’ozone peuvent être émis par les produits de construction et de décoration, et notamment les lambris, puisque ces composés sont émis naturellement par le bois.
Les terpènes mais également les terpénoïdes, composés issus des terpènes, sont fréquemment rencontrés dans les produits d’entretien et les diffuseurs de parfum, de plus en plus utilisés dans les habitations, augmentant ainsi le pourcentage de composés insaturés susceptibles de réagir avec l’ozone [Nazaroff et Weschler, 2004 ; Destaillats et al., 2006a ; Singer et al., 2006]. Les composés fréquemment retrouvés dans la constitution des produits d’entretien et les diffuseurs de parfum d’ambiance sont le camphène, le 3-carène, le d-limonène, les pinènes, l’alpha-phéllandrène, l’alphaterpinolène, l’alpha-terpinène pour la famille des terpènes et le caryophyllène, le longifolène pour les sesquiterpènes. Les terpénoïdes les plus rencontrés sont le citronellon, le gernaiol, le linalool et l’alpha-terpinéol [Nazaroff et Weschler, 2004].
Les produits issus de ces réaction d’ozonolyse peuvent être des ozonides primaires et secondaires, des radicaux libres (Criegee, hydroxyles, alkyles, hydropéroxyles, alkoxyles), des hydropéroxydes des péroxydes d’hydrogène, des péroxy-hémiacétals, des époxydes, des aldéhydes, des cétones, des acides, des composés poly-fonctionnels ou bien encore des aérosols organiques secondaires [Nazaroff et Weschler, 2004]. Certains de ces sous-produits et de produits de réaction se révèlent parfois plus irritants et nocifs que leurs précurseurs, entraînant ainsi la formation d’air de moins bonne qualité [Weschler, 2004]. En terme d’exposition des occupants à des polluants, l’impact sanitaire de ces produits de réaction peut s’avérer plus important que l’ozone ou les COV parents.
Le Tableau ci-après rassemble des sources intérieures fréquentes de composés pouvant réagir avec l’ozone : les occupants, les matériaux, les produits d’entretien, nettoyants et les diffuseurs de parfums d’ambiance. Les composés émis et les principaux produits de réaction stables formés sont également indiqués [Weschler, 2006].
| Source | Emissions | Produits d’ozonolyse stables | ||
|---|---|---|---|---|
| Occupant (air expiré, peau, produits cosmétiques) | isoprène ; NO ; squalène, stérols insaturés ; ac.oléique et autres agi ; produits d’oxydation insaturés | méthacroléine ; mvk ; NO2 ; acétone ; 6-méthyl-5-heptene-2-one ; géranyle acétone ; 4-oxopentanal ; formald. ; nonanal ; décanal ; ac. 9-oxononanoïque, azelaïque et nonanoïque. | ||
| Bois ; Parquet ; Plante d’intérieur | isoprène ; limonène ; alpha-pinène ; autres terpènes et sesquiterpènes | formald. ; pinonald. ; 4-amc ; ac. pinique, pinonique, formique ; méthacroléine ; méthylvinyle cétone ; AOS | ||
| Moquette et leurs envers | 4-phénylcyclohexène ; 4-vinylcyclohexène ; styrène ; 2-éthylhexylacrylate ; acides gras insaturés ; esters | formald. ; acétald. ; benzald. ; hexald. ; nonanal ; 2-nonénal | ||
| Linoléum ; Peinture et Produit à base d’huile de lin | ac. linoléïque et linolénique | propanal ; hexald. ; nonanal ; 2-heptenal ; 2-nonénal ; 2-décénal ; 1-pentèn-3-one ; ac. propionique et n-butyrique | ||
| Peinture | résidus de monomères | formald. | ||
| Produit d’entretien ; Polisseur ; Nettoyant et désodorisant | limonène ; alpha-pinène ; terpinolène ; alphaterpinène ; alpha-terpinéol ; linalool ;linalyl acétate ; longifolène ; autres terpènes, terpénoïdes et sesquiterpènes | formald. ; acétald. ; glycoald. ; ac. formique et acétique ; acétone ; benzaldéhyde ; 4-ydroxy-4- méthyl-5-hexen-1-al ; 5-éthényl-dihydro-5- méthyl-2(3H)furanone ; 4-amc ; AOS | ||
| Adhésif | isoprène ; terpènes | formald. ; méthacroléïne ; méthylvinyle cétone | ||
| Toner de copieur ; Papier | styrène | formald. ; benzald. | ||
| Fumée de tabac | styrène ; acroléine ; nicotine | formald. ; benzald. ; hexald. ; glyoxal ; nméthylformamide ; nicotinald; ; cotinène | ||
| Vêtements et linge de lit usagés | squalène ; stérols insaturés ; ac. oléïque et autres agi | acétone ; géranyleacétone ; 6-méthyl-5-heptene- 2-one ; 4-oxopentanal ; formald. ; nonanal ; décanal ; ac. 9-oxononanoïque, azélaïque et nonanoïque | ||
| Filtres à particules usagés | ac. gras insaturés ; débris végétaux ; suies ; particules diesel | formald. ; nonanal et autres ald. ; ac. azélaïque, nonanoïque, 9-oxononanoïque et autres oxoacides ; composés polyfonctionnels (=O ; - OH ; -COOH) | ||
| Conduit de ventilation | agi et esters ; huiles insaturées ; néoprène | C5 à C10 aldéhydes | ||
| « Déchets urbains » | hap | hap oxydés | ||
| Parfum, eau de Cologne, huile essentielle | limonène ; alpha-pinène ; linalool ; linalyl acétate ; terpinen-4-ol | formald. ; acétone ; 4-amc ; 4-hydroxy-4-méthyl-5-hexen-1-al ; 5-éthenyl-dihydro-5-méthyl-2(3H)furanone ; AOS | ||
| Logement entier | limonène ; alpha-pinène ; styrène | formald. ; pinonald. ; benzald. ; 4-amc ; acétone ; ac. pinique, pinonique, formique ; AOS | ||
| Sources intérieures de substances pouvant subir une ozonolyse et principaux produits de réaction stables hap : hydrocarbures aromatiques polycycliques. -ald. : -aldéhyde. agi : ac. gras insaturés. mvk : méthylvinyl cétone. 4-amc : 4-acétyl-1-méthyl-cyclohexène. |
||||
Mécanismes d'ozonolyse
La présence des produits de réaction est due à une attaque par l’ozone des liaisons carbone–carbone insaturées dans les COV spécifiques, ce type de réaction étant appelé ozonolyse. L’ozone réagit sur ces insaturations pour donner un ozonide primaire qui se décompose rapidement en un composé carbonylé et une espèce radicalaire, avec deux combinaisons possibles. Quelle que soit la combinaison, le carbonyle formé est un aldéhyde, une cétone ou un acide carboxylique. L’espèce radicalaire formée, appelée le radical de Criegee, est énergétiquement très riche et peut à son tour évoluer selon divers mécanismes avec comme espèces intermédiaires très réactives des radicaux hydroxyle, hydroperoxy et alkylperoxy, et comme espèces stables des carbonyles tels que des aldéhydes, des cétones et des acides organiques [Weschler, 2000]. Le mécanisme général d’ozonolyse d’un composé insaturé est présenté ci-dessous.
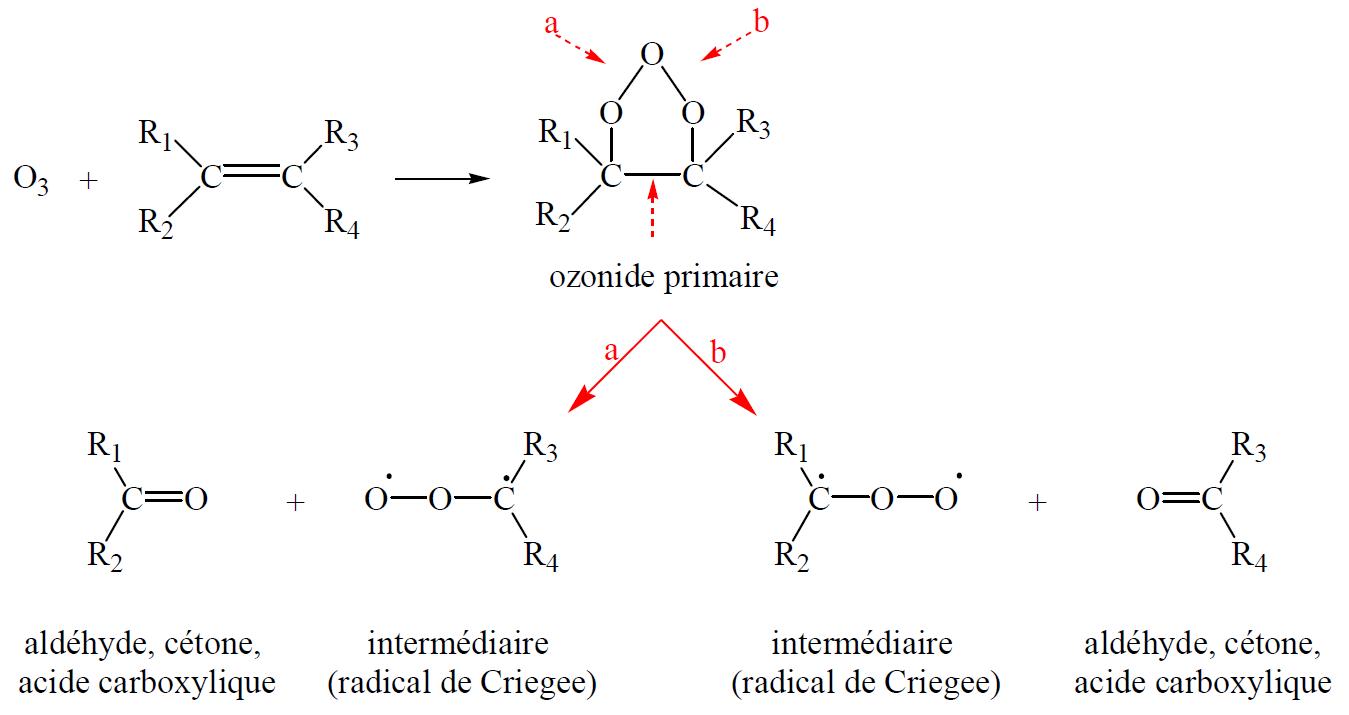
Le mécanisme général d’ozonolyse d’un composé insaturé
Les radicaux de Criegee sont des espèces très réactives pouvant se stabiliser par collision ou se décomposer selon divers mécanismes entraînant la formation du radical hydroxyle [Weschler et Schields, 1997].
Le radical OH· possède un pouvoir oxydant très puissant et peut réagir avec d’autres espèces chimiques, voire même le COV parent ou les COV formés par l’ozonolyse, pour donner de nouveaux composés, stables, contenant un ou plusieurs groupements fonctionnels de type carbonyle, carboxylate et hydroxyle selon le mécanisme suivant :
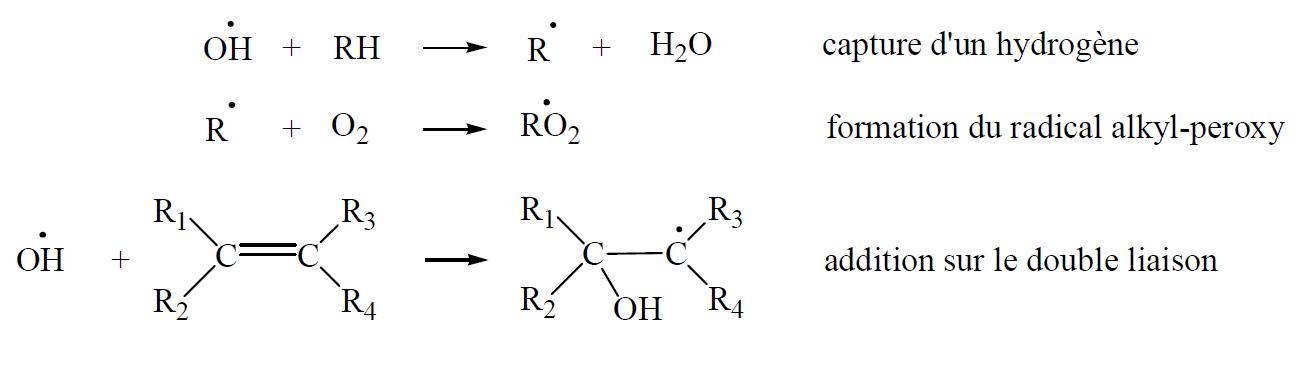
Les rendements de formation du radical hydroxyle sont calculés pour plusieurs terpènes et alcènes, et le Tableau ci-après présente une synthèse des différentes valeurs obtenues.
| Terpènes | Rendement OH· | Références |
|---|---|---|
| Alpha-pinène | 0,77 – 0,85 – 0,70 – 0,83 – 0,91 | Aschamn et al., 2002 – Atkinson et al., 1992 – Paulson et al., 1998 – Rickard et al., 1999 – Siese et al., 2001 |
| Béta-pinène | 0,35 – 0,24 | Atkinson et al., 1992 – Rickard et al., 1999 |
| d-Limonène | 0,67 – 0,86 | Aschamn et al., 2002 – Atkinson et al., 1992 |
| Terpinolène | 0,74 – 1,03 | Aschamn et al., 2002 – Atkinson et al., 1992 |
| Styrène | 0,37 | Atkinson et Aschman, 1993 |
| Rendements de formation du radical hydroxyle pour plusieurs terpènes et alcènes | ||
Produits de réaction
De nombreuses études portent sur les réactions d’ozonolyse des alcènes et notamment des terpènes. Les observations en laboratoire concernent à la fois les composés seuls ou présents en mélange et les sous-produits et produits de ces réactions impliquant l’ozone sont identifiés.
Grosjean et Grosjean [1996] ont étudié la formation de composés carbonylés lors des réactions d’ozonolyse des alcènes, en présence de cyclohexane utilisé pour limiter les réactions impliquant les ions hydroxyles. Les sous-produits et produits de réactions identifiés sont, selon l’alcène considéré, la cyclohexanone, le 2-butanone, le formaldéhyde, le benzaldéhyde, le 2-méthylpropanal, le 2- methylbutanal, le 2,2-dimethylpropanal et l’acétone.
La formation de formaldéhyde, de pinonaldéhyde et de norpinonaldéhyde a été observée par Hatakeyama et al. [1989] après réaction de l’ozone sur l’alpha-pinène et le béta-pinène. En 1998, Yu et al. ont étudié l’ozonolyse de l’alpha-pinène et également mis en évidence la formation de pinonaldéhyde, norpinonaldéhyde et d’acides pinique, pinonique et norpinonique. Une réaction d’ozonolyse de l’alpha-pinène réalisée avec des niveaux de concentrations très importants a été étudiée par Wolkoff et al. [1999a]. La formation de formaldéhyde, de pinonaldéhyde et d’aldéhydes saturés linéaires C2-C6 ainsi que les acides formique et acétique et la méthacroléine a été observée.
Des produits d’ozonolyse de l’alpha-pinène ont été identifiés grâce à une technique de double dérivation au PFBHA – BSTFA [Fick et al., 2003]. Le glyoxal, le méthylglyoxal, le pinonaldéhyde, le norpinonaldéhyde et les acides pinique, pinonique et norpinonique ont été détectés. En absence d’ions hydroxyles, les quantités d’acide pinique, de norpinonaldéhyde et de pinonaldéhyde se sont avérées inférieures et les autres acides n’ont plus été observés. De plus, exception faite du norpinonaldéhyde, une influence de l’humidité est apparue avec une corrélation négative pour l’acide pinonique et positive pour les autres composés.
L’ozonolyse du d-limonène a été étudiée par Glasius et al. [2000] avec comme produits de réaction identifiés les acides limonique, limononique, 7-hydroxylimononique et 7-hydroxy-cétolimononique. Des mélanges de grandes quantités d’isoprène et d’ozone et d’isoprène, d’ozone et de NO2 ont été étudiées par Wilkins et al. [2001]. Le formaldéhyde, l’acétone, la méthyl vinylcétone, la méthacroléine et les acides formique et acétique ont été détectés.
Les techniques classiques d’analyse des produits d’ozonolyse utilisent la chromatographie gazeuse mais une étude concernant la réaction de l’ozone et de plusieurs alcènes et terpènes a présenté des résultat obtenus en spectroscopie infrarouge [Feltham et al., 2000]. La formation d’ozonides issus des réactions impliquant l’éthène, le cis- et le trans-but-2-ène, l’alpha-pinène, le béta-pinène, le 3- carène, le d-limonène et le béta-myrcène a été mise en évidence grâce à cette technique. Une technique de chromatographie liquide associée à la spectrométrie infrarouge a également pu détecter la formation de 7 composés terpénoïdes et d’acides pinique et pinonique lors d’une ozonolyse de l’alpha-pinène [Geiger et al., 2001].
Les produits de réaction issus d’une ozonolyse d’un mélange de 23 COV, représentatifs d’un environnement intérieur classique mais en concentration beaucoup plus importante, ont été analysés [Fan et al., 2003]. La concentration d’ozone employée était de 80 µg·m-3 et la concentration du mélange de COV de 25 mg·m-3. Une augmentation des concentrations de plusieurs aldéhydes a été observée et notamment de formaldéhyde, qui atteint 40 c, mais également d’acétaldéhyde et de propionaldéhyde. De plus, de nouveaux composés ont été détectés : le butyraldéhyde, le glyxoal, le p-tolualdéhyde et le benzaldéhyde, de même que les acides formique et acétique. Lorsque le dlimonène et l’alpha-pinène ont été retirés du mélange de COV, les observations ont été différentes et le seul produit de réaction identifié a été le formaldéhyde (21 µg·m-3).
L’influence de l’ozone, de l’humidité relative et du temps de réaction sur les réactions d’ozonolyse de l’alpha-pinène, du 3-carène et du d-limonène a été étudiée par Fick et al. [2002] à l’aide d’un modèle mathématique. Le classement obtenu par ordre décroissant des différents paramètres, selon leur influence sur les terpènes, a été le suivant : le temps, l’ozone puis l’humidité relative, mais uniquement pour le 3-carène. L’impact de l’humidité est supposé lié à une compétition entre l’eau et l’ozone pour réagir avec le terpène.
Formation d'aérosols organiques secondaires
Les composés stables formés lors de l’ozonisation de composés insaturés peuvent se trouver dans la phase gazeuse mais également dans la phase condensée. Ainsi, en dehors des produits d’ozonolyse précédemment cités, les réactions homogènes induites par l’ozone constituent également des sources d’aérosols organiques secondaires (AOS) [Cocker et al., 2001]. Ces AOS sont principalement des particules submicroniques (<2,5 µm) et constituent un groupe important de produits de réactions initiées par l’ozone. Elles sont formées par les produits d’oxydation dont les pressions de vapeur sont faibles. Ces composés sont partagés entre la phase gazeuse et la surface des aérosols existants ou nouvellement formés par nucléation [Weschler, 2006].
Weschler et Shields [1999] ont mis en évidence l’existence d’une corrélation directe entre les concentrations d’ozone et de terpène et la quantité de particules fines. Différents terpènes (le dlimonène, l’alpha-terpinène et un terpène synthétique issu d’un parfum d’ambiance) ont été introduits séparément dans deux bureaux identiques dont un équipé d’un générateur d’ozone permettant de produire 400 à 600 µg·m-3 d’ozone. Une augmentation importante du nombre de particules a été observée dans le bureau équipé du générateur, la production de particules la plus élevée étant notée avec le d-limonène. Une étude de la réaction entre l’ozone et le d-limonène en tant que source de particules submicroniques a mis en évidence la formation de particules comprises entre 0,1 et 0,2 µm immédiatement après introduction de l’ozone dans la chambre de réaction. Les auteurs ont également étudié l’influence du taux de renouvellement d’air sur la taille et la concentration massique des particules issues de l’ozonolyse du d-limonène [Weschler et Schields, 2003]. Pour un TRA faible, les particules ont présenté des tailles et des masses supérieures, notamment par un temps de séjour plus important amplifiant les interactions particules/composés et les réactions homogènes.
Des mesures de particules ont été réalisées dans six logements à Boston lors de l’utilisation de produits de nettoyage [Long et al., 2000]. En présence d’ozone provenant d’un transfert depuis l’air extérieur, la formation de particules submicroniques a été mise en évidence dans cinq de ces habitations. Les concentrations de particules obtenues ont été 7 à 100 fois plus importantes que la concentration initiale. Près de la moitié de ces particules (en volume) appartenaient à la catégorie des particules ultrafines.
Sarwar et al. [2004] a évalué le rôle des produits de consommation (désodorisant liquide, solide, produits de nettoyage et parfums d’ambiance) dans la formation d’AOS en présence d’ozone. Une augmentation des particules en nombre et en masse est apparue ainsi qu’une diminution de la concentration d’ozone pour chaque essai. Les variations les plus importantes ont été observées pour les produits à base de terpènes. Les auteurs ont ensuite étudié la formation de particules lors de l’ozonolyse de l’alpha-pinène en s’attachant à discriminer la taille des particules formées [Sarwar et al., 2003]. Après introduction de l’ozone dans la chambre d’essai contenant le pinène, les niveaux des particules fines observés ont été supérieurs. Les particules les plus fines (0,02 – 0,1 µm) ont augmenté immédiatement puis diminué au moment où les particules de tailles supérieures (0,1 – 0,2 µm) commencaient à augmenter à leur tour, environ 1½ heure plus tard. L’augmentation des atteindre la taille maximale mesurée (0,5 – 0,7 µm) après environ 10 heures. Wainman et al [2000] ont observé ces mêmes phénomènes lors de l’étude de la réaction d’ozonolyse du d-limonène. Rohr et al. [2003] ont noté lors d’une expérimentation animale sur des souris une importante augmentation des particules ultrafines due à la réaction entre l’ozone et l’alpha-pinène, tous deux présents en concentrations sensiblement supérieures à celles classiquement rencontrées à l’intérieur.
L’ozonolyse d’un mélange de 23 COV classiquement rencontrés à l’intérieur a conduit à une augmentation rapide des particules comprises entre 0,1 et 0,2 µm [Fan et al., 2003].
Hubbard et al. [2005] se sont intéressés à l’impact des générateurs d’ozone sur les particules mesurées dans trois logements (un appartement et deux maisons). La durée de fonctionnement des générateurs variaient de 2 à 5 heures pour des concentrations d’ozone comprises entre 30 et 50 µg·m-3. La source de terpènes provenait d’un produit nettoyant à base d’huile de pin. Lors de l’utilisation du générateur, tous les intervalles de taille de particules ont augmenté avec une taille maximale de 0,7 µm. L’augmentation a commencé par les particules appartenant au plus petit intervalle de taille. Ces particules ont ensuite diminué alors que celles correspondant à l’intervalle de taille suivant commençaient à augmenter.
La réaction d’ozonolyse du styrène a fait l’objet d’investigations par Na et al. [2006] qui ont mis en évidence un rendement de formation d’AOS égal à 12% dans les conditions de leur étude : les concentrations de styrène comprises entre 300 µg·m-3 et 10 mg·m-3 et la concentration d’ozone égale à 800 µg·m-3.
Grosjean et al. [1992, 1993] ont estimé la part d’aérosols formés à 22% lors de la réaction entre l’ozone et le d-limonène.
Destaillats et al. [2006a] ont étudié les polluants secondaires issus des émissions de produits d’usage courant en présence d’ozone à l’aide d’une chambre en téflon de 198 L. Immédiatement après le mélange de tous les réactifs, des évènements de nucléation de particules suivis d’une augmentation significative de taille des particules ont été observés à l’aide d’un analyseur de particules selon le diamètre de leur mobilité électrique, SMPS, (Scanning Mobility Particle Sizer).